Няколко стартиращи компании за милиарди долари се надпреварват да разработят лекарства против стареене, но дали не търсят на грешното място?
В края на 2021 г. руско-израелският милиардер Юри Милнър събира някои от най-известните научни умове на нашето време в пищното си имение на стойност 100 милиона щатски долара в Калифорния. Темата на разговора бе обръщането на процеса на стареенето. Могат ли нашите клетки да бъдат препрограмирани да стават все по-млади? И, може би най-важното за застаряващия милиардер, колко бързо може да бъде разработена тази технология?
Необичайното събитие води до разработването на Altos Labs, биотехнологичен стартъп с амбициите да създаде лечение против стареене, което може да удължи човешкия живот. До следващата година Altos Labs натрупват около 3 милиарда долара финансиране, към което се включват и фигури като Джеф Безос.
Една от ключовите изследователски области, върху които Altos Lab се фокусира, е обръщането на стареенето чрез премахване на епигенетичните маркери, които се натрупват върху клетките с течение на времето. Въз основа на забележителните открития на Шиня Яманака (Shinya Yamanaka) през 2006 г., идеята е, че четири ключови протеина могат да бъдат използвани за изпращане на клетка обратно в нейното ембрионално състояние, като по същество премахват всички биомаркери на стареенето.
Ново проучване от екип биолози и епидемиолози от Калифорнийския университет в Сан Диего (UCLA) поставя под въпрос тази основна основа на много изследвания срещу стареенето. Констатациите предполагат, че фокусирането върху обръщането на епигенетичните маркери може да е грешен подход за опит за обръщане на стареенето, а конкурентна хипотеза за връзката между стареенето и ДНК мутациите може да бъде по-добър подход.
„Големи изследователски институции и компании залагат на връщане на епигенетичния часовник като стратегия за обръщане на ефектите от стареенето, но нашето изследване показва, че това може да е само лечение на симптом на стареенето, а не на основната причина“, обяснява Трей Идекер (Trey Ideker), съавтор на новото проучване. „Ако мутациите действително са отговорни за наблюдаваните епигенетични промени, този факт би могъл да промени фундаментално начина, по който подхождаме към усилията против стареене в бъдеще."
Проучването поставя под въпрос това, което е известно като теория на епигенетичния часовник. В продължение на десетилетия учените са наблюдавали, че химическите промени са склонни да се натрупват в ДНК с напредването на възрастта. Тези промени следват процес, наречен ДНК метилиране. Това е основно механизъм, при който метиловите групи се добавят към сегменти на ДНК, като по същество включват или изключват ген.
През 2011 г. генетикът Стив Хорват (Steve Horvath), заедно с екип от изследователи в UCLA, се насочват към система, която може точно да оцени биологичната възраст на човек въз основа на няколко маркера за метилиране на ДНК в кръвта. Системата е наречена епигенетичен часовник на Хорват и е представена като голяма обединяваща теория за стареенето. Тези епигенетични маркери върху ДНК са нещо повече от низходящ признак на клетъчно стареене, но всъщност движещият фактор зад цял набор от свързани с възрастта клетъчни дисфункции. По принцип тази епигенетична дисрегулация (неспособност за контролиране) на генната експресия е на върха на ефекта на доминото, който засяга клетъчната функция и други дегенеративни процеси. Така че в основата на голяма част от съвременните изследвания против стареене е стремежът да се обърнат или премахнат тези маркери за метилиране, свързани с възрастта. Ако можем да изчистим клетка от тези белези, тогава на теория можем да върнем клетката обратно към младо състояние.
И Хорват, и Яманака са сред многото учени, избрани от Altos Labs да работят върху терапията против стареене.
Епигенетиката
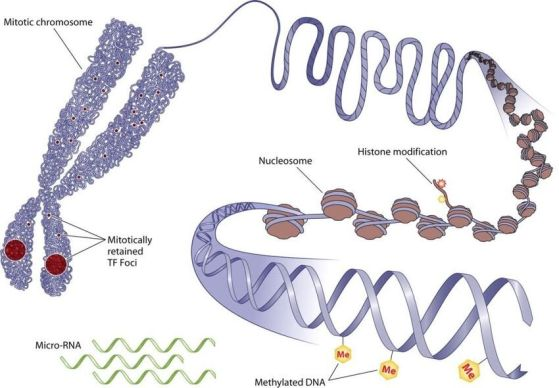
Показани са най-добре проучените епигенетични механизми: ДНК метилиране, хистонова модификация и некодираща РНК-медиирана модулация на генната експресия. Кредит: Zaidi et al. American Society for Microbiology.
Епигенетиката се занимава с изследването на фактори на околната среда, които включват или изключват гените и влияят на това как клетките ще разчитат гените. Тези промени могат да бъдат или да не бъдат наследяеми. Представката „епи-“ произлиза от гръцката επί-, която означава: над, извън, около. Един от епигенетичните механизми, който влияе всеобхватно на човешката физиология е метилирането на ДНК. Той представлява прибавянето на метилови групи (CH3) към 2 от 4-те нуклеотидни бази в молекулата на ДНК. Тази химична реакция променя функцията на ДНК, така че при по-ниски нива на метилиране гените са активни, а при по-високи – не.
„Големи изследователски институции и компании залагат на връщане на епигенетичния часовник като стратегия за обръщане на ефектите от стареенето, но нашето изследване показва, че това може да е само лечение на симптом на стареенето, а не на основната причина“, обяснява Трей Идекер (Trey Ideker), съавтор на новото проучване.
„Ако мутациите действително са отговорни за наблюдаваните епигенетични промени, този факт би могъл да промени фундаментално начина, по който подхождаме към усилията против стареене в бъдеще."
Проучването поставя под въпрос това, което е известно като теория на епигенетичния часовник. В продължение на десетилетия учените са наблюдавали, че химическите промени са склонни да се натрупват в ДНК с напредването на възрастта. Тези промени следват процес, наречен ДНК метилиране. Това е основно механизъм, при който метиловите групи се добавят към сегменти на ДНК, като по същество включват или изключват ген.
През 2011 г. генетикът Стив Хорват (Steve Horvath), заедно с екип от изследователи в UCLA, се насочват към система, която може точно да оцени биологичната възраст на човек въз основа на няколко маркера за метилиране на ДНК в кръвта. Системата е наречена епигенетичен часовник на Хорват и е представена като голяма обединяваща теория за стареенето. Тези епигенетични маркери върху ДНК са нещо повече от низходящ признак на клетъчно стареене, но всъщност движещият фактор зад цял набор от свързани с възрастта клетъчни дисфункции. По принцип тази епигенетична дисрегулация (неспособност за контролиране) на генната експресия е на върха на ефекта на доминото, който засяга клетъчната функция и други дегенеративни процеси. Така че в основата на голяма част от съвременните изследвания против стареене е стремежът да се обърнат или премахнат тези маркери за метилиране, свързани с възрастта. Ако можем да изчистим клетка от тези белези, тогава на теория можем да върнем клетката обратно към младо състояние.
И Хорват, и Яманака са сред многото учени, избрани от Altos Labs да работят върху терапията против стареене.
На теорията на епигенетичния часовник се противопоставя конкурентната „голяма обединяваща теория“ (grand unifying theory), която твърди, че соматичните мутации в ДНК са основната причина за стареенето.
Тази идея предполага, че докато клетките се репликират, естествено възникват мутации и с течение на времето тези мутации се натрупват, причинявайки всички очаквани признаци на стареене. В подкрепа на тази теория бе откритието, че соматичните мутации са склонни да се натрупват по линеен начин през продължителността на живота на повечето видове бозайници. С други думи, проследяването на соматичните мутации се оказва също толкова ефективен начин за измерване на възрастта.
Изследователите се изправят по същество пред въпроса за кокошката или яйцето. Какво е първото? Соматичните мутации или маркерите за метилиране? И каква е връзката между тези два процеса?
Новото изследване засилва тази връзка, изучавайки генетичните данни от повече от 9000 души. То разкрива ясна връзка между соматичните мутации и метилирането на ДНК. Толкова много, че прогнозите за възрастта, направени с помощта на двата показателя, водят до сходни резултати.
Въпреки че може да се докаже, че метилирането на ДНК води до соматични мутации, изследователите отбелязват, че този модел не отчита наблюденията, при които са открити мутации в области на генома с ниски нива на метилиране. С други думи, локалната вероятност от мутации трябва да бъде намалена в присъствието на хипометилиране, ако метилирането е двигател на мутациите. Но това не е това, което изследователите виждат.
Сега изследователите предлагат своя радикална теория – мутациите вероятно са водещият двигател на метилирането на ДНК. И това, което в крайна сметка означава, че работата срещу стареенето, фокусирана върху почистването на клетка от маркери за метилиране, може да бъде безполезна.
„Ако соматичните мутации са основният двигател на стареенето и епигенетичните промени просто проследяват този процес, ще бъде много по-трудно да се обърне стареенето, отколкото смятахме преди“, отбелязва съавторът Стивън Къмингс. „Това измества нашия фокус от разглеждането на стареенето като програмиран процес към такъв, който до голяма степен е повлиян от случайни, кумулативни промени във времето."
Фокусирането върху епигенетичното обръщане може да бъде подобно на лечение на симптом, а не на причина, заключава проучването. Какво означава това за много милиардни проекти срещу стареенето? Скоро ще разберем, когато компании като Altos Labs започнат да прокарват своите експерименти в клинични проучвания. Разбира се, на този етап всичко е само спекулация, но ще бъде ли изненада, ако открием, че обръщането на такъв фундаментален биологичен процес като стареенето е по-трудно, отколкото си мислехме?
Справка: Koch, Z., Li, A., Evans, D.S. et al. Somatic mutation as an explanation for epigenetic aging. Nat Aging (2025). https://doi.org/10.1038/s43587-024-00794-x
Източник: Why Our Biological Clock Ticks: Research Reconciles Major Theories of Aging, University of California San Diego








